目的:探讨葛根素联合银-羟基磷灰石(Ag-HA)涂层植入对种植体周围炎大鼠的炎症水平、骨矿物质密度及骨生物学参数的影响。通过比较不同治疗组的临床表现、炎症因子水平、基因和蛋白表达及骨密度指标为种植体周围炎的治疗提供新的思路和实验依据。
方法:选取雄性大鼠50只为研究对象复制牙周炎模型。模型复制成功后将牙周炎模型大鼠随机分为牙周炎组10只、Ag-HA组20只、联合组20只。牙周炎组大鼠不接受干预,Ag-HA组大鼠接受Ag-HA涂层种植体治疗,联合组大鼠接受葛根素联合Ag-HA涂层种植体治疗。检测并比较术前及术后1、2、4、8周大鼠龈沟出血指数、牙龈指数、探诊深度、血清炎症因子水平、骨结合能力。收集3组大鼠术后8周牙周组织,采用实时荧光定量聚合酶链反应检测相关mRNA的表达,Western blotting检测相关蛋白的表达。对大鼠模
型进行micro CT三维重建后统计并比较骨生物学参数。
结果:牙周炎组、Ag-HA组、联合组术前及术后1、2、4、8周的龈沟出血指、牙龈指数、探诊深度、人肿瘤坏死因子-α(TNF-α)、人白细胞介素-6(IL-6)、人白细胞介素-1β(IL-1β)、碱性磷酸酶(ALP)、骨结合率比较,结果:①不同时间点龈沟出血指、牙龈指数、探诊深度、TNF-α、IL-6、IL-1β、ALP、骨结合率比较,差异均有统计学意义(P <0.05);②牙周炎组、Ag-HA组、联合组龈沟出血指、牙龈指数、
探诊深度、TNF-α、IL-6、IL-1β、ALP、骨结合率比较,差异均有统计学意义(P <0.05),联合组龈沟出血指、牙龈指数、探诊深度、TNF-α、IL-6、IL-1β水平较低,ALP、骨结合能力较高,相对治疗效果较好;③3组龈沟出血指、牙龈指数、探诊深度、TNF-α、IL-6、IL-1β、骨结合率变化趋势比较,差异均有统计学意义(P <0.05);3组骨ALP变化趋势比较,差异无统计学意义(P >0.05)。联合组大鼠牙周组织IL-1β、CXCL12、CXCR4 mRNA和蛋白相对表达量均低于Ag-HA组(P <0.05),OPG mRNA和蛋白相对表达量均高于Ag-HA组(P <0.05)。联合组大鼠组织矿物质密度、骨体积分数、骨小梁厚度均高于Ag-HA组(P <0.05),联合组大鼠骨矿物质密度、上颌第一磨牙釉牙骨质界至牙槽嵴顶的距离均低于Ag-HA组(P <0.05)。
结论:葛根素联合Ag-HA涂层植入能显著改善种植体周围炎大鼠的炎症水平、牙龈指数、探诊深度及骨结合能力。联合治疗较单独治疗在抑制炎症反应、提高骨密度及改善牙周组织修复方面效果更显著。特别是在OPG蛋白表达和骨生物学参数方面,联合治疗表现出较高的优势,提示其在种植体周围炎治疗中的潜在应用价值。
关键词 :种植体周围炎;牙周炎;葛根素;银-羟基磷灰石;大鼠;炎症因子;骨生物学参数
中图分类号 :R783.6
文献标识码 :A
DOI: 10.3969/j.issn.1005-8982.2025.18.006
文章编号:1005-8982 (2025) 18-0032-10
来源:中国知网
(如侵权请联系小编删除)
种植体周围炎是口腔种植修复后常见的并发症,病理特征包括种植体周围软硬组织炎症、骨吸收及微生物生物膜形成,严重时可导致种植体失败。流行病学研究表明,种植体周围炎的发病率高达28%~56%,且与吸烟、糖尿病及口腔卫生不良等因素密切相关[1]。目前临床治疗多依赖机械清创、抗生素应用及局部抗炎药物,但存在疗效有限、易复发及耐药性等问题。因此,开发兼具抗菌、抗炎及骨再生协同作用的治疗策略具有重要临床意义。银-羟基磷灰石(Ag-hydroxyapatite,Ag-HA) 涂层作为一种新型骨植入材料,通过释放银离子Ag+抑制细菌生物膜形成,并通过羟基磷灰石(silver-hydroxyapatite, HA) 的骨传导性促进骨结合,在骨科及牙科领域展现出应用潜力。研究表明,Ag-HA 涂层可显著降低种植体周围金黄色葡萄球菌和铜绿假单胞菌的黏附密度,减轻炎症反应[2]。然而,其对宿主免疫微环境的调控作用及长期骨再生效能仍需进一步验证。葛根素是从豆科植物葛根中提取的异黄酮类化合物, 具有抗炎、抗氧化及免疫调节特性。其作用机制涉及抑制核因子κB (nuclear factor- κB, NF- κB)、丝裂原活化蛋白激酶(mitogen-activated protein kinase, MAPK)及信号转导和转录激活因子(signal transducers and activators of transcription, STAT) 信号通路,减少促炎因子释放,并促进调节性T 细胞分化。动物实验结果显示, 葛根素可通过调控白细胞介素-23(Interleukin-23, IL-23) /辅助性T 细胞17 (T helper cell 17, Th17) 轴抑制破骨细胞活性,改善牙槽骨吸收, 并促进成骨细胞分化及骨矿物质沉积[3-4]。此外,葛根素与纳米材料联合应用可增强生物利用度及靶向性,提示其在骨组织工程中的潜在协同价值。尽管Ag-HA 涂层和葛根素在抗炎及骨修复方面均表现出一定优势,但目前尚无研究探讨两者联合应用对种植体周围炎的综合调控作用。本研究通过构建大鼠种植体周围炎模型,系统评估葛根素联合Ag-HA 涂层植入对炎症因子表达、骨代谢标志物及骨微结构的影响,旨在揭示多靶点联合干预的协同机制,为临床优化种植体周围炎治疗方案提供实验依据。50只SPF级雄性Sprague-Dawley大鼠[实验动物生产许可证号:SCXK (京) 2022-0012],由斯贝福(北京) 生物技术有限公司提供。实验在康复大学青岛中心医院SPF 级动物实验中心完成[实验动物使用许可证号:SYXK (鲁) 2022-0053],所有操作遵循《实验动物护理与使用指南》,并经康复大学实验动物伦理委员会批准。大鼠5~8 周,体重225~255 g。大鼠在稳定环境常规饲养1 周后进行实验,温度22~25 ℃,相对湿度40%~60%。 
HA粉末(瑞士Sulzer Metco公司,粒径15~50 μm),人肿瘤坏死因子- α (tumor necrosis factor, TNF- α)酶联免疫吸附试验(enzyme linked immunosorbent assay, ELISA) 试剂盒(上海酶联生物科技有限公司),人白细胞介素-6 (Interleukin-6, IL-6) 和人白细胞介素-1β (Interleukin-1β, IL-1β) ELISA 试剂盒(上海纪宁生物科技有限公司),RIPA 裂解液(上海康朗生物科技有限公司),蛋白酶/磷酸酶抑制剂、BCA 蛋白浓度检测试剂盒、SDS-PAGE 凝胶配制试剂盒(上海碧云天生物技术股份有限公司),转膜缓冲液(上海万生昊天生物技术有限公司),PVDF/NC 膜(上海迈博瑞生物膜技术有限公司),脱脂奶粉Oxoid? Skim Milk Powder (美国赛默飞世尔科技公司),一抗[C-X-C 基序趋化因子配体12(C-X-C motif chemokine ligand 12, CXCL12)、C-X-C趋化因子受体4 (CXC chemokine receptor 4,CXCR4)、骨保护素(Osteoprotegerin, OPG)、IL-1β](上海艾博抗贸易有限公司),HRP 标记二抗(美国赛默飞世尔科技公司,1∶2 000 稀释),ECL 超敏发光液(北京百奥莱博科技有限公司)。垂直电泳系统电泳仪(北京六一生物科技有限公司),凝胶成像系统(上海嘉鹏科技有限公司,JP-2880 全自动系统),硬组织切片机(德国Exakt公司,E30OCP型),硬组织磨片机(德国Exakt公司,E400CS型),美国西门子Inveon MM CT 系统,Eppendorf 低温离心机(德国艾本德股份公司),恒温孵育摇床(上海智城分析仪器制造有限公司)。 
通过丝线结扎配合10% 高糖饮食进行诱导。具体操作如下:采用5% 水合氯醛腹腔注射后将其固定于仰卧位。轻轻撑开大鼠的上下切牙,清晰暴露出下颌第一与第二磨牙之间的空间。在确保该空间被适当扩张后,使用0.2 mm 正畸结扎丝,巧妙地穿过第一磨牙腭侧的远中邻间隙,再从颊侧穿出,并将其牢固地安置在龈沟内,防止其脱落。饲养过程中,为大鼠提供含10% 高糖水的饮食,并确保每天更换新鲜的食物和水源。为维护结扎丝的稳定性,每3 d 检查1 次,并在发现脱落时立即进行重新结扎。经过8 周的结扎饲养后,对大鼠进行牙周探针检查。该检查包括龈沟出血指数、牙龈指数、探诊深度,每项指标均进行了3 次重复测量,以确保数据的准确性。所有测量均由同一名操作员完成,以消除个体差异对结果的影响。最后根据牙龈炎症的严重程度及牙槽骨的破坏情况来评估模型复制是否成功。确认模型复制成功后,移除结扎丝并恢复常规饮食,采用随机数字表法将模型复制成功大鼠分为3 组:牙周炎组(10 只,无额外干预)、Ag-HA涂层组(20 只) 和联合组(20 只)。Ag-HA 涂层组和联合组大鼠禁食、禁饮12 h 后,肌内注射1.5 mL速眠新进行初步麻醉,10 min 后按1 mL/kg 剂量肌内注射30 g/L 戊巴比妥钠进行深度麻醉。麻醉生效后,对大鼠进行消毒并固定,分别植入Ag-HA 涂层种植体或葛根素联合Ag-HA 涂层种植体,缝合伤口,并术后给予头孢唑啉钠肌内注射预防感染。将高质量的HA 粉末与3% Ag 粉充分混合,混合时长2 h,以确保两种成分均匀分布。利用瑞士Sulzer Metco 真空等离子喷涂技术,在30 mm×30 mm×2 mm的钛合金基材上喷涂形成HA 涂层及含有Ag 抗菌剂的Ag-HA 涂层。喷涂参数: 等离子气体Ar 流量40 L/min,等离子气体H2 流量10 L/min,喷涂距离300 mm,涂层目标厚度200 μm,真空室气压维持在100 Pa, 送粉载气Ar 流量2.0 L/min, 送粉速率20 g/min,电流强度650 A,电压60 V。根据ASTM C-633 标准检测,HA 涂层与Ag-HA 涂层的结合强度分别达到20.1 和23.4 MPa,显示出优异的涂层附着力。Ag-HA 涂层由HA、磷酸三钙、氧化钙及Ag+组成,其中磷酸三钙和氧化钙是在HA 喷涂过程中自然分解产生的。为了进一步优化涂层的性能,采用电化学沉积技术, 在特定的电解液条件下(Ag+浓度0.5 mmol/L,溶液温度40 ℃,pH 4.0,脉冲电位-2 V,沉积时间2 h),将Ag+沉积于HA 涂层表面。沉积完成后,样品在马弗炉中高温处理,升温速率控制在5 ℃/min,以达到所需的热处理效果。随后用大量去离子水(5 L) 洗涤沉淀物,并在70 ℃高温箱中干燥以获得Ag-HA 颗粒。通过玛瑙研磨器研磨至所需粒度。在Ag-HA 涂层的基础上,引入葛根素。按照上述Ag-HA 涂层制备方法,在钛合金基材上形成均匀的Ag-HA 涂层。将葛根素(纯度≥90%) 溶解在乙醇中,浓度控制在1~10 mg/mL,具体浓度可根据所需负载量来调整。将葛根素溶液喷涂在Ag-HA涂层表面,采用喷雾枪或静电喷涂方法,确保均匀覆盖。喷涂时应保持适当的喷涂距离和速率,以确保涂层均匀,不出现过度堆积。葛根素的浓度控制在1~10 mg/mL,根据涂层表面生物活性的需求调整。喷涂可分为2 或3 层进行,每层喷涂后应在室温下静置10~15 min,待溶剂挥发后再进行下一层的喷涂。喷涂完毕后,应将涂层放置在50~60 ℃条件下干燥1 h,以确保溶剂挥发完毕并固定葛根素。固化温度为120~150 ℃,持续30~60 min。选择大鼠下颌第一磨牙缺失区作为植入位点(模拟人类后牙区咬合力需求),该区域牙槽骨高度充足(≥8 mm),骨质致密(皮质骨厚度≥1.5 mm),符合骨结合稳定性要求。通过术前影像学(Micro-CT) 确认植入区无残留牙根或牙槽骨吸收(骨高度≥6 mm),确保为纯骨缺损修复模型。定制钛合金种植体(直径1.8 mm,长度3.0 mm),表面经喷砂酸蚀处理以增强骨结合。使用种植导板将种植体垂直植入骨缺损区, 确保顶端位于皮质骨下0.5 mm (避免穿破上颌窦或下牙槽神经)。通过扭矩控制仪施加15 N·cm 的植入扭矩,达到骨结合所需机械稳定性。种植体完全埋入骨内,颈部无暴露,缝合龈瓣覆盖(使用4-0 可吸收缝线)。术后肌内注射青霉素(8×104 u/kg,连续3 d) 预防感染。术后24 h 禁食,逐步恢复饮水及标准饲料。1.8.1 牙周指标 分别于术前及术后1、2、4、8 周对3 组大鼠牙周指标进行检测。①龈沟出血指数采用6 级分级标准:0 级表示牙龈健康,无炎症或出血迹象;1 级表示牙龈有轻度炎症改变,但探诊时未见出血;2 级为探诊后出现点状出血;3 级为线状出血;4 级为出血溢满并有可能流出龈沟;5 级则表现为牙龈自发性出血。②牙龈指数的测量同样采用4 级分级标准:0 级代表牙龈正常;1 级为轻度炎症,牙龈颜色略有改变并伴有水肿;2 级为中度炎症,牙龈呈现红肿并有出血反应;3 级为重度炎症,牙龈出现红肿或溃疡,且自发性出血明显。牙周探诊深度的测量涵盖了颊侧(近中、中央、远中)和舌侧(近中、中央、远中)共6 个部位。1.8.2 ELISA检测炎症因子水平分别于术前及术后1、2、4、8 周抽取大鼠眦静脉血制备血清,采用ELISA 试剂盒检测血清TNF-α、IL-6、IL-1β水平。1.8.3 ALP、骨结合能力 检测术后1、2、4、8 周3 组大鼠血清碱性磷酸酶(alkaline phosphatase,ALP) 水平。选取Ag-HA 组和联合组大鼠种植体及紧邻3 mm 内骨组织作为样本;牙周炎组则选取牙周炎病灶周边3 mm 内的骨组织。采用美国西门子Inveon MM CT 系统扫描样本。完成扫描后,将种植体周围1 mm 的区域设定为感兴趣区域,以便深入探究种植体与骨组织的结合状态。采用德国Exakt公司E30OCP 型硬组织切片机与E400CS 型硬组织磨片机,以及相应的平行黏合压片装置,制备厚度为30μm的硬组织切片。每个样本选取2张切片以备后续分析。切片制备完毕后,进行亚甲基蓝–酸性品红染色, 以增强样本结构的可视化效果。利用Image-ProPlus 6.0 图像处理软件,对染色后的切片进行图像分析,通过计算得出种植体与骨组织的结合率,以此评估种植体的骨结合效果。

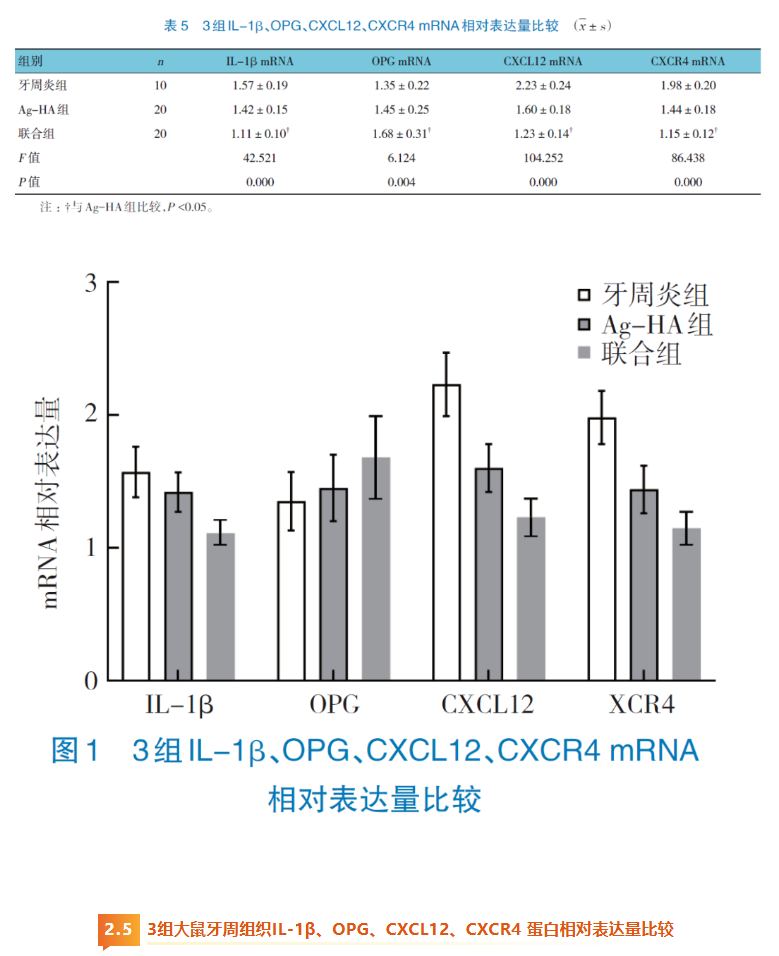
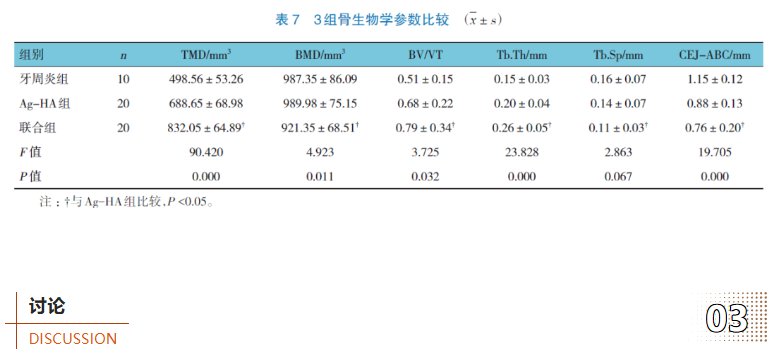
1.8.4 实时荧光定量聚合酶链反应(quantitative realtimepolymerase chain reaction, qRT-PCR)检测mRNA表达术后8 周处死大鼠,收集大鼠牙周组织,使用总RNA 提取试剂盒(北京天根生化科技有限公司,DP419) 提取总RNA。利用FastKing 一步法除基因组cDNA 第一链合成预混试剂(北京天根生化科技有限公司,KR118) 获得cDNA 模板。采用qRT-PCR 检测IL-1β、OPG、CXCL12、CXCR4 mRNA 相对表达量。反应程序为:95 ℃预变性5 s,升温速率4.4 ℃/s。PCR 扩增阶段共40 个循环,每循环包含3 步:95 ℃变性5 s,升温速率4.4 ℃/s;55 ℃退火30 s,升温速率2.2 ℃/s;72 ℃延伸30 s,升温速率2.2 ℃/s。熔解曲线分析阶段:95 ℃维持5 min,升温速率4.4 ℃/s;60 ℃维持1 min,升温速率2.2 ℃/s; 再升温至95 ℃ , 升温速率0.11 ℃/s。降温终止阶段:50 ℃维持30 s,升温速率2.2 ℃/s。引物序列信息见表1。使用2-ΔΔCt 法计算mRNA 相对表达量。1.8.5 Western blotting 检测蛋白表达利用RIPA试剂裂解各组大鼠的牙周组织,提取其中的蛋白质。对提取的蛋白质进行定量处理,确保在进行Western blotting 检测时各组样本的蛋白质浓度一致。进行SDS-PAGE 凝胶电泳,将蛋白质样本分离成不同的组分。电泳完成后, 将蛋白质转移到膜上,以便进行后续的抗体孵育。转膜后使用脱脂乳对膜进行封闭,以减少非特异性结合。4 ℃条件下过夜孵育一抗,一抗包括针对CXCL12、CXR4、OPG、IL-1β 的特异性抗体,所有抗体均以1∶1 000 比例稀释。一抗孵育完成后,将膜在室温下孵育二抗,二抗以1∶2 000 比例稀释,孵育时间为1 h。使用ECL 试剂对膜进行显色,以便观察特异性蛋白的结合情况。利用凝胶成像系统捕捉并保存显色后的图像。通过Image J 软件对图像中的蛋白灰度值进行分析,从而量化各组大鼠牙周组织中各蛋白相对表达量。1.8.6 骨生物学参数将已固定的上颌骨样本使用生理盐水进行全面冲洗,确保其表面无残留物,随后将清洗干净的样本妥善放置于专用的扫描容器内。设置Micro CT 扫描参数:电压70 kV,电流200 mA,曝光时间300 ms,以获取高质量的扫描图像。完成扫描后,利用专业软件进行三维图像重建。在三维重建的图像中, 精确记录以下参数:组织矿物质密度(tissue mineral density, TMD)、骨矿物质密度(bone mineral density, BMD)、骨体积分数(bone volume-to-total volume ratio, BV/TV)、骨小梁厚度(trabecular thickness,Tb.Th)、骨小梁骨分离度(trabecular separation, Tb. Sp)。利用ImageJ 图像分析软件进一步测量上颌第一磨牙釉牙骨质界(cemento-enamel junction, CEJ) 至牙槽嵴顶(alveolar bone crest, ABC) 的距离(CEJ-ABC)。这一测量有助于了解牙周炎对牙周组织的影响程度。数据分析采用SPSS 26.0 统计软件。计量资料以均数±标准差(x±s) 表示,比较用方差分析或重复测量设计的方差分析,两两比较用LSD-t 检验。P <0.05 为差异有统计学意义。牙周炎组、Ag-HA 组、联合组术前及术后1、2、4、8 周的龈沟出血指、牙龈指数、探诊深度比较,采用重复测量设计的方差分析,结果:①不同时间点龈沟出血指、牙龈指数、探诊深度比较,差异均有统计学意义(F =4 340.652、7 635.652、762.759, 均P =0.000); ②牙周炎组、Ag-HA 组、联合组龈沟出血指、牙龈指数、探诊深度比较,差异均有统计学意义(F =3 277.279、4 101.346、759.460,均P =0.000),联合组龈沟出血指、牙龈指数、探诊深度较低,相对治疗效果较好;③3 组龈沟出血指、牙龈指数、探诊深度变化趋势比较,差异均有统计学意义(F =676.317、815.183、156.973,均P =0.000)。见表2。牙周炎组、Ag-HA 组、联合组术前及术后1、2、4、8 周的TNF- α、IL-6、IL-1β 比较,采用重复测量设计的方差分析, 结果: ①不同时间点TNF-α、IL-6、IL-1β 比较,差异均有统计学意义(F =9.777、13.909、9.908,均P =0.000);②牙周炎组、Ag-HA 组、联合组TNF-α、IL-6、IL-1β 水平比较, 差异均有统计学意义(F =17.524、6.379、26.361, 均P =0.000), 联合组TNF- α、IL-6、IL-1β水平较低,相对炎症水平缓解效果较好;③3 组TNF-α、IL-6、IL-1β 水平变化趋势比较,差异均有统计学意义( F=3.489、4.116、4.703,P =0.001、0.000、0.000)。见表3。牙周炎组、Ag-HA 组、联合组术后1、2、4、8 周的ALP、骨结合率比较,采用重复测量设计的方差分析,结果:①不同时间点ALP、骨结合率比较,差异均有统计学意义(F =31.312、1 941.408,均P =0.000); ②牙周炎组、Ag-HA 组、联合组ALP、骨结合率比较,差异均有统计学意义(F =90.924、249.306,均P =0.000),联合组ALP、骨结合能力较高, 相对牙周组织的骨再生能力较强;③3 组骨ALP 变化趋势比较, 差异无统计学意义(F =2.024,P=0.066);骨结合率变化趋势比较,差异有统计学意义(F =75.438,P=0.000)。见表4。牙周炎组、Ag-HA 组、联合组大鼠牙周组织IL-1β、OPG、CXCL12、CXCR4 mRNA 相对表达量比较,经方差分析,差异均有统计学意义(P <0.05);联合组大鼠牙周组织IL-1β、CXCL12、CXCR4 mRNA 相对表达量均低于Ag-HA 组(P <0.05),OPG mRNA 相对表达量高于Ag-HA 组(P <0.05)。见表5 和图1。牙周炎组、Ag-HA 组和联合组大鼠牙周组织IL-1β、OPG、CXCL12、CXCR4 蛋白相对表达量比较,经方差分析,差异均有统计学意义(P <0.05);联合组大鼠牙周组织IL-1β、CXCL12、CXCR4 蛋白相对表达量低于Ag-HA 组(P <0.05),OPG 蛋白相对表达量高于Ag-HA 组(P <0.05)。见图2 和表6。牙周炎组、Ag-HA 组和联合组大鼠TMD、BMD、BV/VT、Tb.Th、CEJ-ABC 比较,经单因素方差分析,差异均有统计学意义(P <0.05);联合组大鼠TMD、BV/VT、Tb. Th 均高于Ag-HA 组(P <0.05),BMD、CEJ-ABC 均低于Ag-HA 组(P <0.05)。见表7。种植体周围炎是种植牙术后影响长期疗效的主要并发症,以种植体周围骨进行性吸收和软组织炎症为特征,可导致种植体松动甚至脱落,严重影响患者口腔功能与生活质量[4-6]。牙菌斑生物膜尤其是革兰阴性厌氧菌如牙龈卟啉单胞菌、具核梭杆菌在种植体表面定植,通过释放毒素激活宿主免疫反应,引发炎症。种植体- 基台微间隙(0.5~1.5 μm) 形成的“死腔效应”进一步促进致病菌富集,加速骨吸收[7]。细菌刺激导致巨噬细胞极化失衡(M1 促炎型占比>85%),释放过量促炎因子(如IL-1β、TNF- α),激活破骨细胞并抑制成骨活性。钛颗粒磨损产物还可激活NLRP3 炎症小体,加剧局部组织破坏[8]。种植体表面粗糙度过高、粘结剂残留、修复体设计不良(如咬合过载);牙周炎病史(风险增加2.5~5 倍)、糖尿病(糖化血红蛋白水平与骨吸收正相关)、吸烟(血管收缩及免疫抑制) [9]。本研究从临床表现来看,联合组大鼠在龈沟出血指数、牙龈指数和探诊深度上的改善均优于牙周炎组和Ag-HA 组。这表明葛根素与Ag-HA 的联合应用能够更有效地减轻种植体周围炎引起的牙龈炎症和牙周袋形成,从而改善牙周组织的健康状况[10]。葛根素具有促进血管生成和细胞增殖的能力,这有助于牙周组织的修复和再生[11]。在种植体周围炎的治疗中,促进牙周组织的修复是恢复其功能的关键[12]。这一结果与ICONARU 等[13]关于葛根素和Ag-HA 各自具有抗炎和促进组织修复作用的研究相一致,但联合应用的效果更显著。联合组大鼠TNF-α、IL-6 和IL-1β水平均显著低于牙周炎组和Ag-HA 组。葛根素通过阻断NLRP3 炎症小体活化, 显著抑制Caspase-1 的切割及IL-1β、IL-18 的成熟释放[14]。实验结果显示,联合组IL-1β蛋白表达较Ag-HA 组降低,这与巨噬细胞极化表型转换密切相关——葛根素促使M1 型促炎巨噬细胞(CD86+) 向M2 型抗炎/修复型(CD206+) 转化。同时,葛根素通过抑制NF- κB 核转位,下调TNF-α、IL-6 等促炎因子转录,减少中性粒细胞浸润及基质金属蛋白酶分泌,从而减少结缔组织降解[15-17]。这一发现进一步支持了葛根素联合Ag-HA涂层植入在牙周炎治疗中的抗炎作用。在骨生物学参数方面,联合组大鼠的ALP 活性、骨结合能力及TMD、BV/VT 和Tb.Th 等指标均优于牙周炎组和Ag-HA 组。ALP 是成骨细胞分化和骨形成的重要标志物,其活性提高表明联合治疗能够促进牙周组织的骨再生[18-20]。同时,骨结合能力增强也验证了联合治疗在促进牙周组织与种植体之间稳定结合方面的优势。此外,TMD、BV/VT 和Tb.Th 等指标提高进一步证明了联合治疗在改善牙周组织骨结构和提高骨密度方面的效果。低剂量Ag+(<2 ppm)可刺激成骨细胞增殖, 而HA 提供骨基质矿化模板。因此联合组BV/TV 和Tb.Th 分别较Ag-HA 组增加,Tb.Sp 降低,证实其可显著改善骨微结构。虽然联合组大鼠BMD 略低于Ag-HA 组,但考虑BMD的变化可能受多种因素的影响,且联合组在其他骨生物学参数上的优势更为显著,因此可以认为这一差异并不影响联合组在牙周炎治疗中的整体效果。CEJ-ABC 在联合组中较低,这可能反映了联合治疗在促进牙周组织修复和重建方面的积极作用,使牙周组织更加接近正常状态[21-24]。联合组大鼠牙周组织中IL-1β表达显著降低,而OPG 表达显著提高。同时,CXCL12 和CXCR4 的表达也发生了变化,这些趋化因子在牙周组织的修复和再生过程中起着重要作用,其表达水平的变化可能反映联合治疗在促进牙周组织细胞迁移和归巢方面的效果[25-26]。综上所述,葛根素联合Ag-HA 涂层植入能够显著改善种植体周围炎大鼠的炎症水平、牙龈指数、探诊深度及骨结合能力。联合治疗在抑制炎症反应、提高骨密度和改善牙周组织修复方面效果更明显。未来的研究可进一步深入研究葛根素联合Ag-HA 涂层植入的机制,并探索其在临床中的应用价值。 [1] 陆丽娟, 刘晓芬. 慢性牙周炎患者种植体周围炎预防的研究进展[J]. 临床口腔医学杂志, 2023, 39(1): 58-60.[2] 王琼, 黄丞一. 赤藓糖醇喷砂治疗牙周病的研究进展[J]. 浙江医学, 2024, 46(14): 1554-1559.[3] GOU H Q, CHEN X, ZHU X M, et al. Sequestered SQSTM1/p62 crosstalk with Keap1/NRF2 axis in hPDLCs promotes oxidative stress injury induced by periodontitis[J]. Free Radic Biol Med,2022, 190: 62-74.[4] PAN Y J, LIN T C, SHAO L Q, et al. Lignin/puerarin nanoparticleincorporated hydrogel improves angiogenesis through puerarininduced autophagy activation[J]. Int J Nanomedicine, 2023, 18:5095-5117.[5] ZHANG G Z, JI J W, SUN M Z, et al. Comparative pharmacokinetic profiles of puerarin in rat plasma by UHPLC-MS/MS after oral administration of Pueraria lobata extract and pure puerarin[J]. J Anal Methods Chem, 2020, 2020: 4258156.[6] SINGH H, KRIPLANI P, KAMBOJ S, et al. Puerarin: an anticancer and anti-inflammatory agent[J]. Recent Pat Anticancer Drug Discov, 2024, 19(1): 18-36.[7] SONG X J, WANG W H, DING S S, et al. Exploring the potential antidepressant mechanisms of puerarin: anti-inflammatory response via the gut-brain axis[J]. J Affect Disord, 2022, 310:459-471.[8] HU R B, DENG L Y, HAO X Y, et al. Direct, broad-spectrum antimicrobial activity of Ag+-doped hydroxyapatite against fastidious anaerobic periodontal and aerobic dental bacteria[J].Materials (Basel), 2024, 17(19): 4688.[9] SILVA-HOLGUÍN P N, REYES-LÓPEZ S Y. Aluminahydroxyapatite- silver spheres with antibacterial activity[J]. Dose Response, 2021, 19(2): 15593258211011337.[10] 万妮, 莫礼文, 詹乐, 等. 葛根素对实验性大鼠牙周炎炎症反应和骨吸收的影响[J]. 海南医学院学报, 2023, 29(8): 575-580.[11] 詹乐, 马瑞堉, 万妮, 等. 葛根素对牙周炎大鼠Th17/Treg 细胞免疫平衡及相关转录因子表达的影响[J]. 昆明医科大学学报,2022, 43(11): 36-43.[12] WU J Y, HUANG Y X, ZHAN C, et al. Thioredoxin-1 promotes the restoration of alveolar bone in periodontitis with diabetes[J]. iScience, 2023, 26(9): 107618.[13] ICONARU S L, PREDOI D, CIOBANU C S, et al. Development of silver doped hydroxyapatite thin films for biomedical applications[J]. Coatings, 2022, 12(3): 341.[14] WANG J P, WANG X F, LIANG Z W, et al. Injectable antibacterial Ag-HA/ GelMA hydrogel for bone tissue engineering[J]. Front Bioeng Biotechnol, 2023, 11: 1219460.[15] LI J, PENG Y J. Effect of puerarin on osteogenic differentiation of human periodontal ligament stem cells[J]. J Int Med Res,2020, 48(4): 300060519851641.[16] LUO W, SUN L. O-Linked N-Acetylglucosamine transferase regulates bone homeostasis through alkaline phosphatase pathway in diabetic periodontitis[J]. Mol Biotechnol, 2024,66(12): 3475-3484.[17] ZHOU H, QI Y X, ZHU C H, et al. Mesenchymal stem cellderived extracellular vesicles for treatment of bone loss within periodontitis in pre-clinical animal models: a meta-analysis[J]. BMC Oral Health, 2023, 23(1): 701.[18] YAN K X, LIN Q, TANG K L, et al. Substance P participates in periodontitis by upregulating HIF-1α and RANKL/OPG ratio[J].BMC Oral Health, 2020, 20(1): 27.[19] JIANG W T, XU T, SONG Z M, et al. CCL2 is a key regulator and therapeutic target for periodontitis[J]. J Clin Periodontol,2023, 50(12): 1644-1657.[20] JIANG W T, XU T, YUAN S S, et al. Critical roles for CCR2 and the therapeutic potential of cenicriviroc in periodontitis: a pre-clinical study[J]. J Clin Periodontol, 2022, 49(11): 1203-1216.[21] 高巍朕, 张晓鹏, 李文科. 自体软组织移植辅助前牙即刻种植对唇侧轮廓美学的影响[J]. 中国现代医学杂志, 2025, 35(4):54-59.[22] LIU X C, DENG S D, LI X Y, et al. A standardized rat model to study peri-implantitis of transmucosal osseointegrated implants[J]. Biomater Res, 2024, 28: 0021.[23] 王培, 苏小营, 后岷红. 上颌前牙区牙槽骨缺损形态与种植修复术后植骨吸收率的相关性及影响移植骨吸收的因素分析[J]. 中国现代医学杂志, 2023, 33(4): 6-10.[24] WANG X G, CHEN X T, ZHANG Z X, et al. Asperuloside prevents peri-implantitis via suppression of NF-κB and ERK1/2 on rats[J]. Pharmaceuticals (Basel), 2022, 15(8): 1027.[25] CAFFERATA E A, RAMANAUSKAITE A, CUYPERS A, et al. Experimental peri-implantitis induces neuroinflammation: an exploratory study in rats[J]. BMC Oral Health, 2024, 24(1):1238.[26] 黄大海, 王祥芸, 储雯, 等. IL-6 对种植体周围炎大鼠牙龈组织中TNF-α 表达的影响[J]. 河北医药, 2024, 46(15): 2256-2260.
[1] 陆丽娟, 刘晓芬. 慢性牙周炎患者种植体周围炎预防的研究进展[J]. 临床口腔医学杂志, 2023, 39(1): 58-60.[2] 王琼, 黄丞一. 赤藓糖醇喷砂治疗牙周病的研究进展[J]. 浙江医学, 2024, 46(14): 1554-1559.[3] GOU H Q, CHEN X, ZHU X M, et al. Sequestered SQSTM1/p62 crosstalk with Keap1/NRF2 axis in hPDLCs promotes oxidative stress injury induced by periodontitis[J]. Free Radic Biol Med,2022, 190: 62-74.[4] PAN Y J, LIN T C, SHAO L Q, et al. Lignin/puerarin nanoparticleincorporated hydrogel improves angiogenesis through puerarininduced autophagy activation[J]. Int J Nanomedicine, 2023, 18:5095-5117.[5] ZHANG G Z, JI J W, SUN M Z, et al. Comparative pharmacokinetic profiles of puerarin in rat plasma by UHPLC-MS/MS after oral administration of Pueraria lobata extract and pure puerarin[J]. J Anal Methods Chem, 2020, 2020: 4258156.[6] SINGH H, KRIPLANI P, KAMBOJ S, et al. Puerarin: an anticancer and anti-inflammatory agent[J]. Recent Pat Anticancer Drug Discov, 2024, 19(1): 18-36.[7] SONG X J, WANG W H, DING S S, et al. Exploring the potential antidepressant mechanisms of puerarin: anti-inflammatory response via the gut-brain axis[J]. J Affect Disord, 2022, 310:459-471.[8] HU R B, DENG L Y, HAO X Y, et al. Direct, broad-spectrum antimicrobial activity of Ag+-doped hydroxyapatite against fastidious anaerobic periodontal and aerobic dental bacteria[J].Materials (Basel), 2024, 17(19): 4688.[9] SILVA-HOLGUÍN P N, REYES-LÓPEZ S Y. Aluminahydroxyapatite- silver spheres with antibacterial activity[J]. Dose Response, 2021, 19(2): 15593258211011337.[10] 万妮, 莫礼文, 詹乐, 等. 葛根素对实验性大鼠牙周炎炎症反应和骨吸收的影响[J]. 海南医学院学报, 2023, 29(8): 575-580.[11] 詹乐, 马瑞堉, 万妮, 等. 葛根素对牙周炎大鼠Th17/Treg 细胞免疫平衡及相关转录因子表达的影响[J]. 昆明医科大学学报,2022, 43(11): 36-43.[12] WU J Y, HUANG Y X, ZHAN C, et al. Thioredoxin-1 promotes the restoration of alveolar bone in periodontitis with diabetes[J]. iScience, 2023, 26(9): 107618.[13] ICONARU S L, PREDOI D, CIOBANU C S, et al. Development of silver doped hydroxyapatite thin films for biomedical applications[J]. Coatings, 2022, 12(3): 341.[14] WANG J P, WANG X F, LIANG Z W, et al. Injectable antibacterial Ag-HA/ GelMA hydrogel for bone tissue engineering[J]. Front Bioeng Biotechnol, 2023, 11: 1219460.[15] LI J, PENG Y J. Effect of puerarin on osteogenic differentiation of human periodontal ligament stem cells[J]. J Int Med Res,2020, 48(4): 300060519851641.[16] LUO W, SUN L. O-Linked N-Acetylglucosamine transferase regulates bone homeostasis through alkaline phosphatase pathway in diabetic periodontitis[J]. Mol Biotechnol, 2024,66(12): 3475-3484.[17] ZHOU H, QI Y X, ZHU C H, et al. Mesenchymal stem cellderived extracellular vesicles for treatment of bone loss within periodontitis in pre-clinical animal models: a meta-analysis[J]. BMC Oral Health, 2023, 23(1): 701.[18] YAN K X, LIN Q, TANG K L, et al. Substance P participates in periodontitis by upregulating HIF-1α and RANKL/OPG ratio[J].BMC Oral Health, 2020, 20(1): 27.[19] JIANG W T, XU T, SONG Z M, et al. CCL2 is a key regulator and therapeutic target for periodontitis[J]. J Clin Periodontol,2023, 50(12): 1644-1657.[20] JIANG W T, XU T, YUAN S S, et al. Critical roles for CCR2 and the therapeutic potential of cenicriviroc in periodontitis: a pre-clinical study[J]. J Clin Periodontol, 2022, 49(11): 1203-1216.[21] 高巍朕, 张晓鹏, 李文科. 自体软组织移植辅助前牙即刻种植对唇侧轮廓美学的影响[J]. 中国现代医学杂志, 2025, 35(4):54-59.[22] LIU X C, DENG S D, LI X Y, et al. A standardized rat model to study peri-implantitis of transmucosal osseointegrated implants[J]. Biomater Res, 2024, 28: 0021.[23] 王培, 苏小营, 后岷红. 上颌前牙区牙槽骨缺损形态与种植修复术后植骨吸收率的相关性及影响移植骨吸收的因素分析[J]. 中国现代医学杂志, 2023, 33(4): 6-10.[24] WANG X G, CHEN X T, ZHANG Z X, et al. Asperuloside prevents peri-implantitis via suppression of NF-κB and ERK1/2 on rats[J]. Pharmaceuticals (Basel), 2022, 15(8): 1027.[25] CAFFERATA E A, RAMANAUSKAITE A, CUYPERS A, et al. Experimental peri-implantitis induces neuroinflammation: an exploratory study in rats[J]. BMC Oral Health, 2024, 24(1):1238.[26] 黄大海, 王祥芸, 储雯, 等. IL-6 对种植体周围炎大鼠牙龈组织中TNF-α 表达的影响[J]. 河北医药, 2024, 46(15): 2256-2260.















 扫一扫 关注我们
扫一扫 关注我们