

患有牙髓坏死和根尖周病变的牙齿,其根管系统具有复杂的微生物环境。微生物可以在根管壁上形成生物膜结构,并进入峡部,侧支根管等器械以及冲洗液难以到达的部位,包括牙本质小管[1]。细菌对牙本质小管的侵袭可以在2/3的牙本质厚度中被检测到[2]。这些部位中的残余感染会成为再感染或持续感染的根源[2?3]。近年来研究表明,使用冲洗活化技术的策略可以显著影响冲洗液对牙本质小管的渗透。与常规注射器冲洗(conventional syringe irrigation,CSI)相比,被动超声冲洗(passive ultrasonic irrigation,PUI)、新型声波冲洗、激光活化冲洗均可增加冲洗液对牙本质小管的渗透深度,改善根管消毒效果[4?5]。虽然已有关于根管冲洗液对牙本质小管渗透的研究,但这些研究中所用样本都是动物牙齿[6]、人类清洁根管状态牙齿[7],或体外接种微生物的感染牙本质模型[8],与临床感染根管的结构和微生物环境存在差异[9?10]。目前尚无研究以人牙感染根管作为研究对象来评估不同动力冲洗活化技术对根管冲洗液进入牙本质小管渗透性的影响。因此,本研究以临床感染根管为研究对象,体外评估被动超声冲洗和Er:YAG激光活化冲洗(Er: YAG laser and photon?induced photoacoustic streaming,PIPS)对人牙感染根管牙本质的渗透效果。
1.1 主要材料和仪器
手用锉(Mani,Tochigi,日本);光固化流动树脂Z350(3M ESPE,美国);机用旋转镍钛器械(VDW GmbH,德国);3% NaOCl溶液(齿博士,中国);17% EDTA(朗力,中国);被动超声冲洗(P5Newtron,Servotome,法国);Er:YAG 激光光子诱导光声流技术(Fotona,德国);2%亚甲基蓝溶液(Sigma?Aldrich,德国);EXAKT 硬组织切磨系统(EXAKT® Apparatebau GmbH & Co,德国);光学显微镜(Zeiss Axio?phot,德国)。

1.2 研究对象
选择对牙髓活力测试无反应和影像学资料显示存在牙髓来源的根尖阴影的感染根管36例(因残根残冠拔除),根据冲洗方式随机分组(CSI 组12例、PUI组12例、PIPS组12例);选择牙髓活力测试正常且影像学资料显示牙齿硬组织及根尖周无异常情况的清洁根管36例(因正畸原因拔除),根据冲洗方式随机分组(CSI 组12 例、PUI 组12 例、PIPS组12例)。所有纳入根管均为后牙的直根管,避免根管弯曲对冲洗液渗透的影响。去除牙齿表面软组织及牙石,清洗洁净后,储存于10%福尔马林中备用。本试验通过安徽医科大学附属口腔医院伦理委员会审批(审批号:T2022021)。
1.3 根管体外机械预备
1.3.1 标准化牙根长度
用金刚砂片在牙骨质和牙釉质交界处截取牙根,牙根长度标准化为10 ~15 mm。
1.3.2 测量根管工作长度
使用手用锉8 号0.02锥度至20 号0.02 锥度通畅根管,根管工作长度为通畅长度减去1 mm。使用光固化流动树脂Z350覆盖所有实验牙的根尖端,避免冲洗液溢出并模拟体内根尖受根尖周组织保护的解剖条件。
1.3.3 机械预备
使用机用旋转镍钛器械进行根管预备,所有根管均预备至40 号0.06 锥度。预备过程中,每更换一次镍钛器械,都使用3% NaOCl溶液冲洗,在室温下,冲洗剂量为1 mL,冲洗时间为30 s。
所有实验牙齿储存在超纯水中。
1.4 根管动态活化冲洗
准备3%NaOCl(55 ℃)、无菌生理盐水和17%EDTA。所涉及冲洗技术为常规注射器冲洗、被动超声冲洗(功率7 W,无水)和Er:YAG 激光光子诱导光声流技术(SSP模式,15 Hz,0.3 W)。
冲洗策略如下:① 3%NaOCl(5 mL,1 min);② 无菌生理盐水(5 mL,1 min);③ 17%EDTA(5 mL,1 min),活化冲洗30 s,间歇期30 s,两个循环;④ 生理盐水(5 mL,1 min);⑤ 3%NaOCl(15 mL,3 min),活化冲洗30 s,间歇期30 s,6个循环[11?13]。
1.5 样本染色
干燥后于牙齿表面涂布无色油漆以避免牙齿的外表面着色。在根管中注入2%亚甲基蓝溶液,活化1 min,以可视化冲洗剂的渗透深度[13]。吸潮纸尖干燥根管后,用光固化流动树脂Z350充填根管的冠方入口。牙齿干燥储存。
1.6 样本切片和光镜观察
使用EXAKT 硬组织切磨系统在每颗牙齿的冠、中、根尖1/3 处获取100 ~ 150 μm 厚度的横向切片[7]。在光学显微镜下观察所有切片并拍照,将图片导入ImageJ 软件分析。
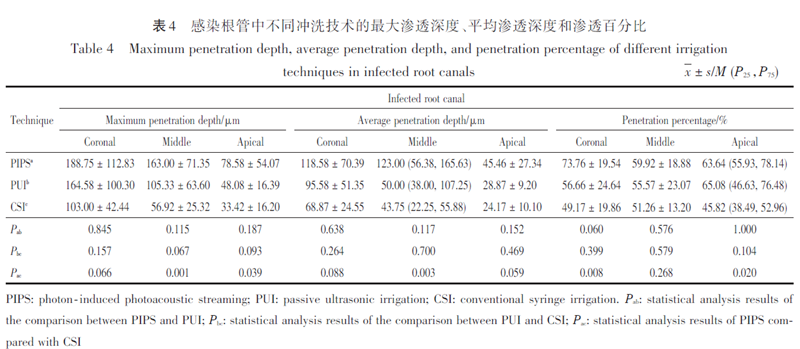
图1为染色和切片后的代表性图像。为评估冲洗液对牙本质小管的渗透,在每张切片上测量以下量化指数:最大渗透深度、平均渗透深度和渗透百分比,渗透百分比=(染色根管壁周长/根管壁总周长)×100%。
1.7 统计学分析
采用SPSS 23.0 统计学软件分析数据,计量资料若符合正态分布,采用均数± 标准差(x ± s)表示,两组间比较用t 检验,多组间比较用方差分析;计量资料若不符合正态分布,采用M(P25,P75)表示,组间比较用非参数检验。P<0.05为差异具有统计学意义。
2.1 根部牙本质的渗透性分析
3 种冲洗技术下,在根部牙本质的全长,感染根管的最大渗透深度、平均渗透深度、渗透百分比均小于清洁根管,差异均有统计学意义(P<0.05,表1、2、3)。
2.2 不同动力冲洗技术对感染牙本质中冲洗液渗透性的影响
在感染根管的冠方,PIPS 组的渗透百分比大于CSI组(P<0.05);PUI组和CSI组的渗透深度和渗透百分比差异无统计学意义(P>0.05);PIPS组和PUI组的渗透深度和渗透百分比差异无统计学意义(P>0.05,表4)。在感染根管的根中部,PIPS组的最大渗透深度以及平均渗透深度均大于CSI组(P<0.05);PUI组和CSI组的渗透深度和渗透百分比差异无统计学意义(P>0.05);PIPS 组和PUI组的渗透深度和渗透百分比差异无统计学意义(P>0.05)。在感染根管的根尖,PIPS组的最大渗透深度以及渗透百分比均大于CSI 组(P<0.05);PUI组和CSI组的渗透深度和渗透百分比差异无统计学意义(P>0.05);PIPS 组和PUI 组的渗透深度和渗透百分比差异无统计学意义(P>0.05)。
根尖周炎是由感染根管系统内微生物诱导的感染性疾病[1]。即使进行规范化根管治疗,根尖周炎的治疗失败率仍可高达15%,而其根本原因依然是感染的残留[14?15]。感染根管复杂的微生物环境会增加治疗难度,如果根管感染无法得到有效控制,持续性根尖周炎的发生会给根管治疗带来困难,而对于免疫功能低下的患者,感染有全身传播的风险[16?17]。因此,研究感染根管的感染控制策略具有重要的临床意义。
目前对于感染根管的治疗策略主要是通过机械预备和化学预备来降低根管系统内的细菌负荷,从而诱导根尖周病变愈合[18?19]。在根管机械预备后,仍有65%的牙齿的牙本质小管被细菌侵袭[20],所以根管系统的化学预备对感染根管的成功清创和消毒起着至关重要的作用,而如何促进冲洗液对牙本质小管的渗透是目前化学预备中研究的热点。
虽然近年来已经有较多的研究关注于次氯酸钠冲洗液在根管中的渗透情况[21?23],但是,聚焦于临床感染根管的研究资料尚待完善。本研究选取临床感染根管为研究对象,观察次氯酸钠溶液在感染根管牙本质中的渗透深度,结果显示感染根管的牙本质渗透性弱于清洁根管;Er:YAG 激光冲洗活化技术可显著改善次氯酸钠溶液对感染牙本质的渗透效果。感染牙本质渗透性较差的原因可能是牙本质小管的硬化。小管硬化是随年龄增长发生的管周牙本质的生理性沉积,并逐渐由根尖向冠方形成[24];小管硬化也可由病理刺激诱导形成,如龋齿等[25]。小管硬化会阻碍染料对牙本质小管的渗透,是影响牙本质渗透性的主要因素[26]。在感染根管中,不仅可以发生小管硬化的生理性沉积,而且在感染根管形成期间,长期的病理过程同样可以诱导小管硬化的形成,而清洁根管中却无此病理诱导过程,由此,造成了两者渗透性的差异。此结果进一步加深了感染根管的临床感染控制难度的认识,在临床实践中,应该探索渗透性能更好的冲洗策略,从而改善根管消毒效果。
虽然研究表明激光和超声动力冲洗技术能够有力地促进根管冲洗液在牙本质小管中的渗透[27?29],但是,其应用于临床感染根管的研究资料仍有待补充。本研究同样分析了两种动力冲洗技术对次氯酸钠溶液在感染根管中渗透效果的影响,在感染根管状态下,与常规注射器冲洗相比,Er:YAG激光活化冲洗可以显著改善次氯酸钠溶液对感染牙本质的渗透深度和渗透百分比,而被动超声冲洗并未显著改善次氯酸钠溶液对感染牙本质的渗透深度和渗透百分比。此结果与Galler等[13]和Olivi 等[30]的研究结果相似,PIPS在牙本质切片中实现了更深的牙本质小管渗透。PIPS可以显著促进抗菌冲洗液的渗透,从而获得更好的牙髓治疗效果[31],带有PIPS尖端的Er:YAG激光动力冲洗技术基于其光声效应和光机械作用,使得脉冲可与水分子广泛反应以构成膨胀冲击波和连续冲击波,从而促进液体流动,而且PIPS的纤维尖端放置在髓腔内,不需要插入根管尖端,更适应于弯曲狭窄的根管,可与根管系统的复杂性相匹配[23,32]。将PIPS 应用于感染根管的活化冲洗中,可以提升临床感染控制效果。
本研究的缺陷在于所涉及样本的年龄不明。年龄不仅影响根部牙本质的渗透性[33],而且影响根管的感染程度[34],所以未来在感染根管渗透性的相关研究中应加入对年龄的考虑。
感染根管的牙本质渗透性弱于清洁根管;Er:YAG激光动力冲洗活化技术可以显著改善次氯酸钠溶液对感染牙本质的渗透效果;推荐将Er:YAG激光活化冲洗技术用于感染根管的治疗。
[1] Siqueira JF Jr, Rôças IN. Present status and future directions: Microbiology of endodontic infections [J]. Int Endod J, 2022, 55(Suppl 3): 512?530. doi: 10.1111/iej.13677.
[2] Vera J, Siqueira JF Jr, Ricucci D, et al. One? versus two?visit endodontic treatment of teeth with apical periodontitis: a histobacteriologic study [J]. J Endod, 2012, 38(8): 1040?1052. doi: 10.1016/j.joen.2012.04.010.
[3] Zandi H, Petronijevic N, Mdala I, et al. Outcome of endodontic retreatment using 2 root canal irrigants and influence of infection on healing as determined by a molecular method: a randomized clinical trial [J]. J Endod, 2019, 45(9): 1089?1098.e5. doi: 10.1016/j.joen.2019.05.021.
[4] Plotino G, Grande NM, Mercade M, et al. Efficacy of sonic and ultrasonic irrigation devices in the removal of debris from canal irregularities in artificial root canals [J]. J Appl Oral Sci, 2019, 27:e20180045. doi: 10.1590/1678?7757?2018?0045.
[5] Bordea IR, Hanna R, Chiniforush N, et al. Evaluation of the outcome of various laser therapy applications in root canal disinfection: a systematic review [J]. Photodiagnosis Photodyn Ther, 2020,29: 101611. doi: 10.1016/j.pdpdt.2019.101611.
[6] Faria G, Viola KS, Coaguila?Llerena H, et al. Penetration of sodium hypochlorite into root canal dentine: effect of surfactants, gel form and passive ultrasonic irrigation [J]. Int Endod J, 2019, 52(3): 385?392. doi: 10.1111/iej.13015.
[7] Virdee SS, Farnell DJJ, Silva MA, et al. The influence of irrigant activation, concentration and contact time on sodium hypochlorite penetration into root dentine: an ex vivo experiment [J]. Int Endod J, 2020, 53(7): 986?997. doi: 10.1111/iej.13290.
[8] Villalta?Briones N, Baca P, Bravo M, et al. A laboratory study of root canal and isthmus disinfection in extracted teeth using various activation methods with a mixture of sodium hypochlorite and etidronic acid [J]. Int Endod J, 2021, 54(2): 268?278. doi: 10.1111/iej.13417.
[9] Ortiz?Ruiz AJ, de Dios Teruel?Fernández J, Alcolea?Rubio LA, et porcine, and ovine teeth [J]. Ann Anat Anat Anzeiger, 2018, 218: 7 17. doi: 10.1016/j.aanat.2017.12.012.
[10] Dehghani Nazhvani A, Dehghanpour Frashah H, Haddadi P, et al.Ultrastructural and chemical composition of dentin and enamel in lab animals [J]. J Dent (Shiraz), 2019, 20(3): 178 ? 183. doi:10.30476/DENTJODS.2019.44912.
[11] Ate? AA, Ar?can B, Çiftçio?lu E, et al. Influence of different irrigation regimens on the dentinal tubule penetration of a bioceramicbased root canal sealer: a confocal analysis study [J]. Lasers Med Sci, 2021, 36(8): 1771?1777. doi: 10.1007/s10103?021?03356?4.
[12] Mozgovaya LA, Kosolapova EY, Godovalov AI, et al. Morphology of root dentine in teeth extracted because of chronic apical periodontitis in various irrigation protocols [J]. Stomatologiia (Mosk),2020, 99(2): 7?10. doi: 10.17116/stomat2020990217.
[13] Galler KM, Grubmüller V, Schlichting R, et al. Penetration depth of irrigants into root dentine after sonic, ultrasonic and photoacoustic activation [J]. Int Endod J, 2019, 52(8): 1210 ? 1217. doi:10.1111/iej.13108.
[14] Siqueira JF Jr, Rôças IN, Riche FNSJ, et al. Clinical outcome of the endodontic treatment of teeth with apical periodontitis using an antimicrobial protocol [J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endodontology, 2008, 106(5): 757?762. doi: 10.1016/j.tripleo.2008.06.007.
[15] Ricucci D, Russo J, Rutberg M, et al. A prospective cohort study of endodontic treatments of 1, 369 root canals: results after 5 years [J]. Oral Surg Oral Med Oral Pathol Oral Radiol Endodontology,2011, 112(6): 825?842. doi: 10.1016/j.tripleo.2011.08.003.
[16] Nagendrababu V, Segura?Egea JJ, Fouad AF, et al. Association between diabetes and the outcome of root canal treatment in adults:an umbrella review [J]. Int Endod J, 2020, 53(4): 455?466. doi:10.1111/iej.13253.
[17] Niazi SA, Bakhsh A. Association between endodontic infection, its treatment and systemic health: a narrative review [J]. Medicina (Kaunas), 2022, 58(7): 931. doi: 10.3390/medicina58070931.
[18] Moyin S, Punathil S, Pulyodan MK, et al. An Ex vivo evaluation of antimicrobial efficacy of root canal preparation with hand K?files, hand pro taper, and pro taper rotary files [J]. J Pharm Bioallied Sci, 2019, 11(Suppl 2): S305?S308. doi: 10.4103/JPBS.JPBS_19_19.
[19] Prada I, Micó?Muñoz P, Giner?Lluesma T, et al. Update of the therapeutic planning of irrigation and intracanal medication in root canal treatment. A literature review [J]. J Clin Exp Dent, 2019, 11(2): e185?e193. doi: 10.4317/jced.55560.
[20] Matsuo T, Shirakami T, Ozaki K, et al. An immunohistological study of the localization of bacteria invading root pulpal walls of teeth with periapical lesions [J]. J Endod, 2003, 29(3): 194?200.doi: 10.1097/00004770?200303000?00008.
[21] Iandolo A, Abdellatif D, Amato M, et al. Dentinal tubule penetration and root canal cleanliness following ultrasonic activation of in?tracanal?heated sodium hypochlorite [J]. Aust Endod J, 2020, 46(2): 204?209. doi: 10.1111/aej.12393.
[22] Coaguila?Llerena H, Barbieri I, Tanomaru?Filho M, et al. Physicochemical properties, cytotoxicity and penetration into dentinal tubules of sodium hypochlorite with and without surfactants [J]. Restor Dent Endod, 2020, 45(4): e47. doi: 10.5395/rde.2020.45.e47.
[23] Kosarieh E, Bolhari B, Sanjari Pirayvatlou S, et al. Effect of Er:YAG laser irradiation using SWEEPS and PIPS technique on dye penetration depth after root canal preparation [J]. Photodiagnosis Photodyn Ther, 2021, 33: 102136. doi: 10.1016/j.pdpdt.2020.102136.
[24] Yan W, Jiang E, Renteria C, et al. Odontoblast apoptosis and intratubular mineralization of sclerotic dentin with aging [J]. Arch Oral Biol, 2022, 136: 105371. doi: 10.1016/j.archoralbio.2022.105371.
[25] Yoshihara K, Nagaoka N, Nakamura A, et al. Three?dimensional observation and analysis of remineralization in dentinal caries lesions [J]. Sci Rep, 2020, 10(1): 4387. doi: 10.1038/s41598?02061111?1.
[26] Paqué F, Luder HU, Sener B, et al. Tubular sclerosis rather than the smear layer impedes dye penetration into the dentine of endodontically instrumented root canals [J]. Int Endod J, 2006, 39(1):18?25. doi: 10.1111/j.1365?2591.2005.01042.x.
[27] Tungsawat P, Arunrukthavorn P, Phuntusuntorn P, et al. Comparison of the effect of three irrigation techniques and root canal preparation size on sodium hypochlorite penetration into root canal dentinal tubules [J]. Int J Dent, 2021, 2021: 6612588. doi: 10.1155/2021/6612588.
[28] Rajakumaran A, Ganesh A. Comparative evaluation of depth of penetration of root canal irrigant after using manual, passive ultrasonic, and diode laser?assisted irrigant activation technique [J]. J Pharm Bioallied Sci, 2019, 11(Suppl 2): S216?S220. doi: 10.4103/JPBS.JPBS_300_18.
[29] Subramani SM, Anjana G, Raghavan I, et al. Evaluation of antimicrobial efficacy and penetration depth of various irrigants into the dentinal tubules with and without lasers: a stereomicroscopic study [J]. Int J Clin Pediatr Dent, 2019, 12(4): 273 ? 279. doi:10.5005/jp?journals?10005?1647.
[30] Olivi M, Raponi G, Palaia G, et al. Disinfection of root canals with laser ? activated irrigation, photoactivated disinfection, and combined laser techniques: an ex vivo preliminary study [J]. Photobiomodul Photomed Laser Surg, 2021, 39(1): 62?69. doi: 10.1089/photob.2020.4879.
[31] Do QL, Gaudin A. The efficiency of the Er: YAG laser and PhotonInduced photoacoustic streaming (PIPS) as an activation method in endodontic irrigation: a literature review [J]. J Lasers Med Sci, 2020, 11(3): 316?334. doi: 10.34172/jlms.2020.53.
[32] Damade Y, Kabir R, Gaddalay S, et al. Root canal debridement efficacy of heated sodium hypochlorite in conjunction with passive ultrasonic agitation: an ex vivo study [J]. J Dent Res Dent Clin Dent Prospects, 2020, 14(4): 235?238. doi: 10.34172/joddd.2020.040.
[33] Thaler A, Ebert J, Petschelt A, et al. Influence of tooth age and root section on root dentine dye penetration [J]. Int Endod J, 2008, 41(12): 1115?1122. doi: 10.1111/j.1365?2591.2008.01486.x.
[34] Kakoli P, Nandakumar R, Romberg E, et al. The effect of age on bacterial penetration of radicular dentin [J]. J Endod, 2009, 35(1): 78?81. doi: 10.1016/j.joen.2008.10.004.










 扫一扫 关注我们
扫一扫 关注我们